
~~~ La versione in italiano inizia subito dopo la versione in inglese ~~~
ENGLISH

14-08-2025-Materials Technologies - States of Aggregation [EN]-[IT] With this post, I would like to provide a brief introduction to the topic mentioned in the article. (code notes: X-95-94-93-92-91-90)
States of Aggregation

Image created with artificial intelligence, the software used is Microsoft Copilot
Introduction Matter can exist in various forms: solid, liquid, or gaseous. We can therefore say that the states of matter describe the forms in which matter can exist. Technically, it would be correct to say that the properties of the different states of matter are due to the different nature of the interaction forces between particles. These interaction forces occur between atoms, molecules, and ions.
State Changes
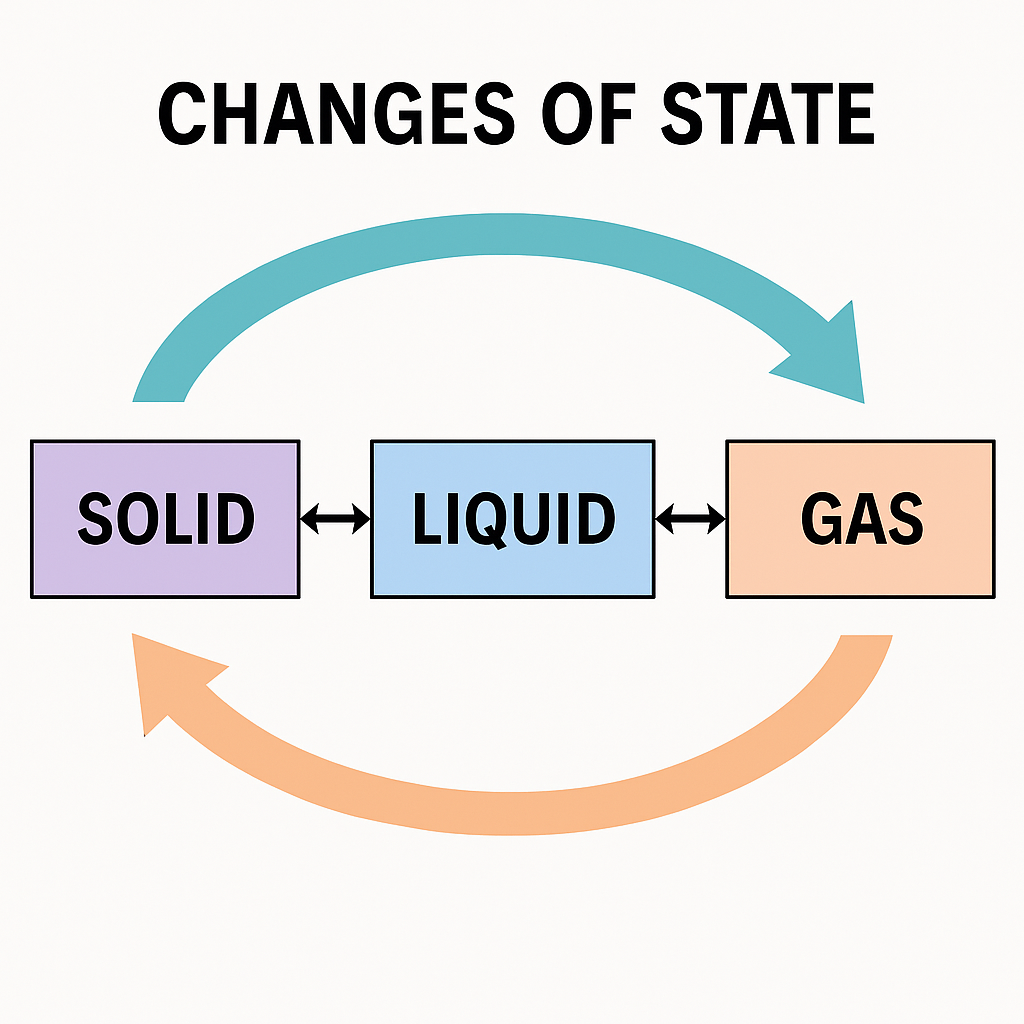
The same chemical species can generally exist in different states of aggregation depending on its pressure and temperature. Therefore, state changes are those transitory moments in which matter passes from one state of aggregation to another.
The transition from one state of matter to another
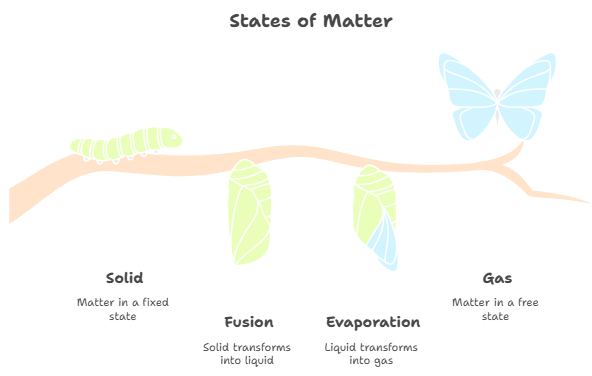
Image created with artificial intelligence, the software used is Napkin.ai
To explain the transitions from one state to another, let's start with one parameter: temperature. Let's imagine the temperature increasing. Let's start from the solid state; our matter has solidified, but the temperature begins to rise. Then the phase called fusion begins, and the matter becomes liquid. At this point, the temperature continues to increase. The phase called evaporation begins, and here the matter transforms into vapor or gas.
The reverse journey, matter changing from vapor to solid
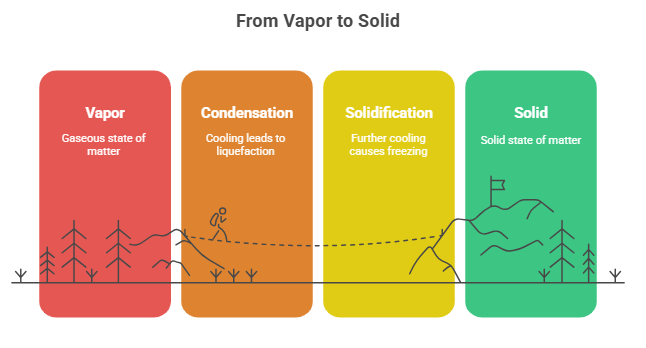
Image created with artificial intelligence, the software used is Napkin.ai
When matter is in the vapor or gas state and the temperature drops, the liquefaction or condensation phase begins. The matter will now appear as a liquid. Lowering the temperature further will result in solidification, and the matter will change from a liquid to a solid state.
Sublimation and Frost
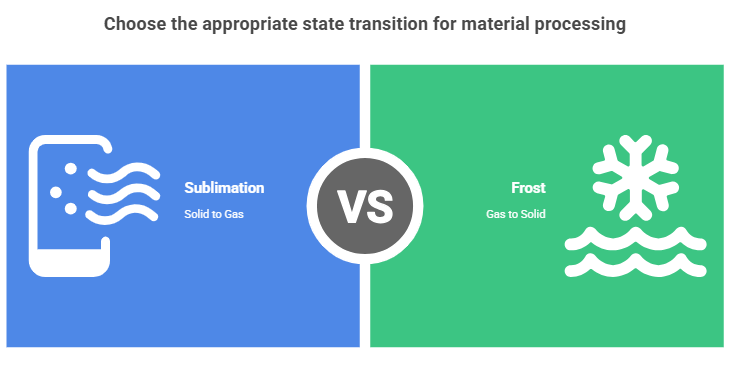
Image created with artificial intelligence, the software used is Napkin.ai
Who hasn't heard of sublimation or frost? However, we might be unsure of what they are exactly. Sublimation and frost are two very specific state transitions. Sublimation Sublimation occurs when a material passes directly from the solid state to the gaseous state, bypassing the liquid phase. For example, dry ice, which would otherwise be solid CO₂, turns into a gas at –78.5°C. Hoarfrost Hoarfrost occurs when a material passes directly from the gaseous state to the solid state, bypassing the liquid phase. The most classic example is frost, a phenomenon in which water vapor from the air deposits directly as ice on cold surfaces.
Gaseous, Liquid, and Solid States
Gaseous State A gas is a system composed of a very large number of particles (atoms or molecules) in chaotic motion. There are two main categories of gases: ideal gases and real gases. The main difference between ideal and real gases is that in the latter, the particles have a significant volume compared to that of their container, and that interactions exist between the particles that compose it, however weak.
Liquid State A liquid is a system composed of particles in chaotic motion, between which attractive forces act. Their strength is such that they cannot separate, but they are insufficient to hold them in fixed positions, like those of a crystal lattice. This state of aggregation can be seen as an intermediate state between gas and solid. Liquids have several characteristics that distinguish them from gases. Below, I describe what I consider to be the four main differences. Liquids: - have a well-defined surface, although they are not rigid. - their volume remains practically constant as the temperature increases. - are practically incompressible. - molecules are in constant, disordered motion, which is why they always assume the shape of the container containing them.
Solid State This state is characterized by the fact that the particles of matter are close together and, above all, ordered. The structure can be crystalline, meaning regularly arranged (as in metals, for example), or amorphous (as in glass, for example).
Unlike the gaseous or liquid state, the particles do not move freely, but vibrate around fixed positions.
Conclusions States of aggregation are extremely important for the use and transformation of materials. When studying materials, the solid, liquid, and gaseous states are distinguished by the arrangement and interaction of particles, strongly influencing the physical and technological properties of a material.
Question We can say that materials technology was also a pursuit pursued by ancient civilizations, such as those of the Neolithic, but did you know that Agricola (1494-1555) and Galileo (1564-1642) are considered the true first scholars of materials technology?

ITALIAN

14-08-2025-Tecnologie dei materiali - Stati di aggregazione [EN]-[IT] Con questo post vorrei dare una breve istruzione a riguardo dell’argomento citato in oggetto (code notes: X-95-94-93-92-91-90)
Stati di aggregazione

immagine creata con l’intelligenza artificiale, il software usato è Microsoft Copilot
Introduzione La materia si può trovare in varie forme, solido, liquido o gassoso. Possiamo quindi dire che gli stati di aggregazione descrivono le forme in cui può trovarsi la materia. Tecnicamente sarebbe corretto dire che le proprietà dei diversi stati di aggregazione sono dovute alla diversa natura delle forze di interazione fra le particelle. Queste forze di interazione avvengono tra gli atomi, le molecole e gli ioni.
I passaggi di stato

Una stessa specie chimica generalmente può presentarsi in diversi stati di aggregazione a seconda della pressione e della temperatura a cui essa si trova. Quindi i passaggi di stato sono quei momenti transitori in cui la materia passa da uno stato di aggregazione all'altro.
Il passaggio da uno stato di aggregazione all'altro

immagine creata con l’intelligenza artificiale, il software usato è Napkin.ai
Per spiegare i passaggi da uno stato all'altro partiamo da un parametro, la temperatura. Immaginiamo di avere la temperatura crescente. Iniziamo dallo stato solido, quindi la nostra materia è solidificata, ma la temperatura inizia ad alzarsi. Inizia quindi la fase chiamata fusione e la materia diventa liquida A questo punto la temperatura continua ad aumentare. Inizia la fase chiamata evaporazione e qui la materia si trasforma in vapore o gas.
Il viaggio inverso, la materia che passa dal vapore al solido

immagine creata con l’intelligenza artificiale, il software usato è Napkin.ai
Quando la materia è nello stato di vapore o gas e la temperatura si abbassa, inizia la fase di liquefazione o condensazione. La materia ora si presenterà in forma di liquido. Abbassando ulteriormente la temperatura avremo la solidificazione e la materia passerà dallo stato liquido a quello solido.
Sublimazione e brinamento

immagine creata con l’intelligenza artificiale, il software usato è Napkin.ai
Chi non ha mai sentito parlare di sublimazione o brinamento? Potremmo però avere dei dubbi su cosa possano essere in maniera precisa. La sublimazione ed il brinamento sono due transizioni di stato molto particolari. Sublimazione La sublimazione avviene quando il materiale passa direttamente dallo stato solido allo stato gassoso, saltando la fase liquida. Esempio il ghiaccio secco che sarebbe CO₂ solida, esso si trasforma in gas a –78,5 °C. Brinamento La brinamento avviene quando il materiale passa direttamente dallo stato gassoso allo stato solido, saltando anche qui la fase liquida. L'esempio più classico è quello della brina, fenomeno in cui il vapore acqueo dell’aria si deposita direttamente come ghiaccio su superfici fredde.
Stato gassoso, liquido e solido

Stato gassoso Il gas è un sistema costituito da un numero elevatissimo di particelle (atomi o molecole) animate da moto caotico. Le categorie dei gas sono principalmente due, i gas ideali e i gas reali. La principale differenza tra gas ideale e reale è che in quest’ultimo le particelle hanno volume proprio non trascurabile rispetto a quello del loro contenitore e che tra le particelle che lo compongono, per quanto deboli, esistono interazioni.
Stato liquido Il liquido è un sistema costituito da particelle animate da moto caotico tra le quali agiscono forze attrattive di entità tale da non consentirne la separazione, ma insufficienti a bloccarle in posizioni fisse come quelle di un reticolo cristallino. Questo stato di aggregazione può essere visto come uno stato intermedio tra quello gassoso e quello solido. I liquidi hanno diverse caratteristiche che li distinguono dai gas, qui di seguito descrivo quelle che io ritengo come quelle che possono essere definite le quattro principali differenze. I liquidi: - presentano una superficie ben definita sebbene non siano dotati di rigidità - con l’aumentare della temperatura il volume rimane praticamente costante - sono praticamente incomprimibili - le molecole sono dotate di costante e disordinato movimento, per questo assumono sempre la forma del recipiente che le contiene.
Stato solido Questo stato è caratterizzato dal fatto che le particelle della materia sono vicine e soprattutto ordinate. La struttura può essere cristallina, cioè di ordine regolare (come ad esempio nei metalli) o amorfa (come ad esempio nel vetro) Differentemente dallo stato gassoso o liquido, qui le particelle non si spostano liberamente, ma vibrano attorno a posizioni fisse.
Conclusioni Gli stati di aggregazione assumono un'importanza estrema per l'uso dei materiali o la trasformazione di essi. Quando siamo nell'ambito dello studio dei materiali, gli stati solido, liquido e gassoso si distinguono per disposizione e interazione delle particelle, influenzando fortemente le proprietà fisiche e tecnologiche di un materiale.
Domanda Possiamo dire che la tecnologia dei materiali era una ricerca che facevano anche le civilizzazioni antiche, come quelle del Neolitico, ma lo sapevate che Agricola (1494-1555) e Galileo (1564-1642) sono visti come i veri e primi studiosi della tecnologia dei materiali?
THE END
immagine creata con l’intelligenza artificiale, il software usato è Napkin.ai