Hola amigos
En el post anterior presenté información relacionada con la molaridad, siendo esta una unidad de concentración de la solución denotada por la letra “M” que indica la cantidad de moles de un soluto presentes en un volumen de solución expresado en litros.
#
Recordemos que a partir de la molaridad se pueden realizar cálculos que involucran moles de soluto, masa molar y volumen. Ahora bien, como sabemos resulta importante conocer las distintas formas en que se pueden determinar las concentraciones de las soluciones, es por ello que en esta oportunidad quiero mostrar cómo a partir de un análisis volumétrico se puede determinar la concentración de una solución expresada en molaridad, ya que constituye uno de los análisis que comúnmente se realiza en un laboratorio y es necesario dominar los cálculos involucrados y las unidades respectivas.
**Imagen realizada en power point** @yusvelasquez
Un análisis volumétrico es un análisis cuantitativo que se basa en la medición del volumen de una solución de concentración conocida que reacciona por con el analito.
Uno de los métodos volumétricos más empleados es el de neutralización en donde reacciona un ácido y una base cuya reacción involucrada es la siguiente:
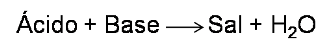
En este tipo de valoraciones el analito puede ser una solución básica y la solución titulante un ácido o viceversa, se emplea un indicador para detectar el punto final y se mide el volumen gastado en la titulación para realizar los cálculos correspondientes.
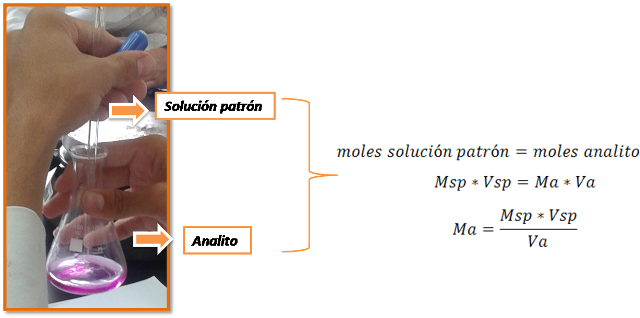
**Fuente: @yusvelasquez**
Ahora bien **¿Cómo se determina la molaridad de la solución a partir de la titulación?**
Un procedimiento sencillo para determinar la concentración de un ácido o una base consiste en los siguientes pasos:
En primer lugar se calcula la cantidad en moles de titulante a partir del volumen añadido y su concentración. Se escribe la ecuación química balanceada de la reacción de neutralización. Se expresa la relación estequiométrica entre el analito y el titulante para la conversión de la cantidad de titulante en cantidad de analito. Finalmente se calcula la molaridad del analito tomando en cuenta el volumen inicial de la solución.
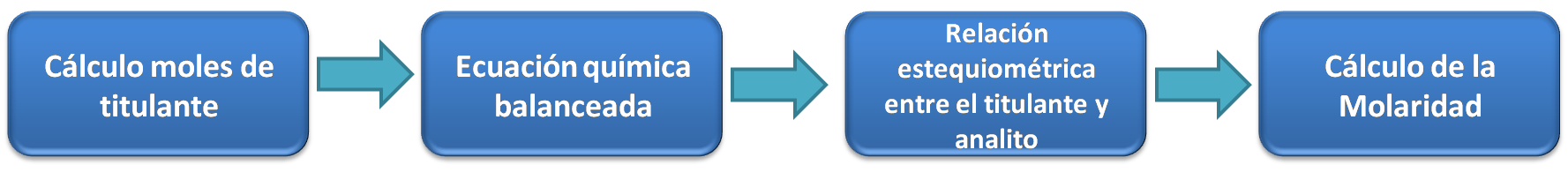
_Veamos algunos ejemplos del cálculo de la molaridad siguiendo el procedimiento descrito anteriormente._
**_Ejemplo 1_**. Supongamos que en una valoración de 15 mL de Hidróxido de sodio NaOH se gastaron 17.40 mL de HCl 0.234 M. ¿Cuál es la molaridad del hidróxido de sodio?
En este primer ejemplo el titulante corresponde al ácido clorhídrico y el analito el hidróxido de sodio por lo que siguiendo los pasos, los cálculos involucrados son:
- moles de titulante a partir del volumen gastado en la titulación y su concentración.
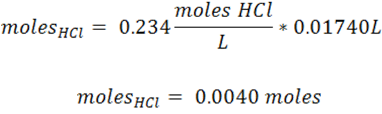
- Reacción de titulación

- Relación estequiométrica
Como vemos la relación estequiométrica es 1:1 lo que indica que 1 mol de ácido reacciona con 1 mol del hidróxido de sodio
- Cálculo de la molaridad
La molaridad del hidróxido de sodio se calcula partiendo de los moles de titulante y la relación estequiométrica establecida para convertir los moles de titulante en moles de analito y se divide entre el volumen inicial. El cálculo viene dado por:
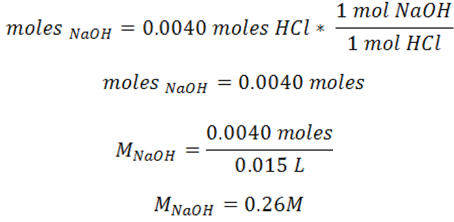
**_Ejemplo 2_**. Supongamos que en una valoración se empleó una solución de HCl que contenía 0.72g de HCl en 500mL para titular 25mL de Ca(OH)2 y se gastaron 15.1mL de ácido.¿Cuál será la molaridad de la solución del hidróxido de calcio?
Como vemos, en este caso no se cuenta con la molaridad del titulante (HCl), por lo que se debe determinar en primer lugar de la siguiente forma empleando la masa molar y el volumen:
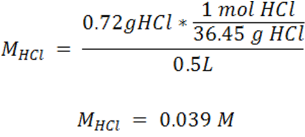
Posteriormente se puede proceder con los pasos descritos anteriormente.
- moles de HCl
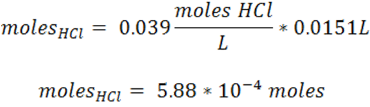
- Reacción de titulación
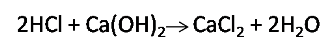
- Relación estequiométrica entre el ácido y la base
Como vemos la relación estequiométrica indica que 2 moles de ácido reaccionan con 1 mol del hidróxido de calcio.
- Cálculo de la molaridad
La molaridad del hidróxido de calcio se calcula partiendo de los moles de titulante y la relación estequiométrica para convertir los moles de titulante en moles de analito y se divide entre el volumen inicial. El cálculo viene dado por:
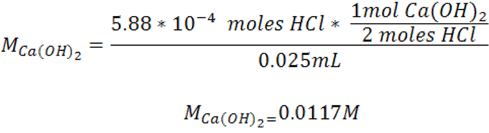
En el caso de la determinación de la molaridad de un ácido se puede proceder de forma similar siguiendo los pasos descritos.
Como puede observarse en estos casos, los cálculos de la molaridad de una solución a partir de la titulación se basan en la concentración del titulante, el volumen gastado en la titulación y el volumen de la solución del analito.
Los métodos volumétricos de neutralización constituyen uno de los métodos de laboratorio más utilizados por ser rápidos, precisos, permite determinar la concentración de gran cantidad de ácidos y bases o en otro casos se pueden someter analitos a tratamiento químico para su conversión en especies ácidas o básicas y su posterior análisis.
#### Hasta una próxima oportunidad, gracias por leer
### Referencias
- Atkins, J. (2006). Principios de Química. Los caminos del descubrimiento.
- Skoog, W.(2000) Química Analítica. Mc Graw Hill